La ricerca scientifica, spinta da un’incessante curiosità e dalla volontà di superare i limiti del conosciuto, ha recentemente varcato soglie precedentemente inesplorate nel campo della biologia riproduttiva umana. Al centro di queste scoperte si trova l’ovulo umano non fecondato, un elemento biologico che, in circostanze straordinarie e attraverso sofisticate manipolazioni, sta aprendo scenari inediti per la comprensione della vita e per potenziali applicazioni terapeutiche. Questo articolo si propone di esplorare a fondo i meccanismi, le implicazioni e le controversie che circondano l'attivazione e lo sviluppo di ovuli non fecondati, noti anche come partenoti, andando oltre la mera definizione per addentrarsi nelle complesse sfaccettature scientifiche, etiche e legali che caratterizzano questo affascinante campo di indagine.
La Partenogenesi: Una "Nascita Vergine" Artificiale
Il concetto di partenogenesi, letteralmente "nascita vergine" in greco, non è una novità assoluta nel regno biologico. Questa modalità riproduttiva asessuata è infatti osservata in natura in numerose specie vegetali e animali, tra cui api, formiche e alcune specie di lucertole. Tuttavia, nei mammiferi, e quindi anche nell'uomo, la partenogenesi naturale è impedita da un complesso meccanismo di regolazione genica noto come "imprinting genomico". L'imprinting assicura che l'embrione si sviluppi correttamente richiedendo il contributo genetico sia della madre che del padre. In assenza di questo doppio apporto, lo sviluppo completo è compromesso.
Nonostante questo ostacolo naturale, gli scienziati hanno compiuto passi da gigante nell'indurre artificialmente la partenogenesi in mammiferi, inclusi topi e primati. La ricerca condotta dal gruppo di Paul de Sousa presso l'Università di Edimburgo, operante presso il Roslin Institute - lo stesso istituto che ha visto la nascita della pecora clonata Dolly - rappresenta un esempio emblematico di tale progresso. Utilizzando circa 300 ovuli umani donati volontariamente, il team è riuscito a creare una mezza dozzina di blastocisti partenoti. Queste strutture, costituite da circa 50 cellule, rappresentano un potenziale serbatoio di cellule staminali, aprendo così la strada a una nuova era nella ricerca e nella medicina rigenerativa.
Il processo per ottenere questi partenoti umani è stato meticoloso. Normalmente, un ovulo umano, preparandosi alla fecondazione, espelle metà del suo materiale genetico. Per creare i partenoti, gli ovuli sono stati coltivati in laboratorio in modo da conservare tutti i loro cromosomi. Successivamente, circa la metà di questi ovuli è stata sottoposta a uno shock elettrico, una procedura volta a maturarli e indurre la divisione cellulare. Nonostante questi sforzi, solo una piccola percentuale (cinque su cento) è riuscita a raggiungere lo stadio di blastocisti, presentando un numero di cellule inferiore rispetto a una blastocisti derivata da fecondazione naturale. Il dottor De Sousa ha sottolineato che, nonostante queste sfide, il "gioco numerico" è sufficiente a fornire il "tessuto che dovrà essere impiegato nella sperimentazione".
L'Imprinting Genomico: Un Complesso Interruttore Biologico
Per comprendere appieno le sfide e le potenzialità della partenogenesi umana, è fondamentale approfondire il concetto di imprinting genomico. Questo fenomeno biologico distingue i geni "marcati" (imprinted) da quelli che seguono le comuni regole ereditarie. L'imprinting stabilisce che l'espressione di un gene dipenda dal genitore da cui è stato ereditato. In pratica, la maggior parte dei geni imprinted viene repressa, il che significa che solo la copia materna o paterna di un particolare gene viene effettivamente espressa.
Questo sofisticato meccanismo ha origine durante la formazione dei gameti (ovuli e spermatozoi). Nei maschi, alcuni geni subiscono l'imprinting nello sperma in via di sviluppo, mentre nelle femmine, altri geni subiscono lo stesso processo nell'ovulo. Tutte le cellule dell'embrione che ne risulterà erediteranno lo stesso set di geni imprintati da entrambi i genitori, ad eccezione delle cellule germinali (destinate a produrre ovuli o spermatozoi), in cui tutti gli imprint vengono cancellati.
L'importanza dell'imprinting è tale che una sua alterazione può avere conseguenze gravi. L'eredità di due copie di un cromosoma da un solo genitore, o l'assenza di una copia dall'altro, è spesso fatale. Allo stesso modo, l'eredità di due copie di un gene materno e nessuna copia di quello paterno (o viceversa) può portare a gravi difetti di sviluppo. Ancora più preoccupante è il legame tra la mancanza di imprinting nelle cellule somatiche e lo sviluppo del cancro.
La ricerca sui partenoti, che per definizione mancano dell'imprinting paterno, riveste quindi un interesse scientifico cruciale. Studiare questi embrioni artificiali potrebbe fornire preziose informazioni sulla clonazione - un processo che a sua volta interferisce con l'imprinting - e sui complessi legami tra imprinting difettoso e insorgenza di patologie.
Applicazioni Terapeutiche e Potenziale per la Ricerca
Le implicazioni della ricerca sulla partenogenesi umana vanno ben oltre la mera curiosità scientifica. La capacità di generare partenoti apre scenari promettenti per la coltura di tessuti e cellule femminili, con potenziali applicazioni in una vasta gamma di esperimenti e cure.
Uno degli ambiti più entusiasmanti è quello della medicina rigenerativa. In teoria, le cellule staminali ottenute da partenoti potrebbero essere impiegate per coltivare tessuti di sostituzione destinati a donne affette da determinate patologie. Questo potrebbe rivoluzionare il trattamento di condizioni che attualmente presentano opzioni terapeutiche limitate.
Inoltre, la partenogenesi offre la possibilità di coltivare cellule da donne affette da gravi malattie genetiche. Questo permetterebbe uno studio dettagliato degli effetti cellulari di queste malattie, fornendo ai ricercatori un modello prezioso per comprendere i meccanismi patologici e sviluppare nuove strategie terapeutiche.
Nonostante queste potenzialità, il dottor De Sousa ha ammesso che il suo gruppo non è ancora riuscito a ottenere cellule staminali da questi embrioni, pur mantenendo questa ambizione come obiettivo primario.
Cellule Staminali : Il Futuro Della Cura È Qui #scienza #medicina #consapevolezza #psicologia
Dibattito Etico e Legale: Tra Innovazione e Protezione
L'avanzamento della ricerca sulla partenogenesi umana solleva inevitabilmente questioni etiche e legali complesse. La possibilità di creare embrioni senza la fecondazione tradizionale ha suscitato reazioni contrastanti da parte di gruppi pro-vita e della comunità scientifica.
Alcuni scienziati avevano ipotizzato che l'impiego dei partenoti nella ricerca potesse aggirare le obiezioni etiche dei gruppi pro-vita, poiché questi organismi non derivano dalla fecondazione di un ovulo con uno spermatozoo. Tuttavia, le dichiarazioni di sgomento rilasciate da tali gruppi alla stampa hanno dimostrato che questa ipotesi era infondata. Il dottor De Sousa stesso ha riconosciuto che "chi ha un atteggiamento a favore della vita considererà opinabile qualsiasi utilizzo di ovuli ed embrioni a fini non riproduttivi".
È importante sottolineare che il gruppo di Edimburgo non ha alcuna intenzione di impiantare gli embrioni partenoti per indurre una gravidanza. Tale eventualità è espressamente vietata dalle clausole della licenza di ricerca concessa al team.
Altri hanno sollevato dubbi di natura tecnica, sostenendo che il livello di manipolazione genetica necessario per la partenogenesi rende questo percorso eccessivamente complicato per ottenere cellule staminali embrionali. Secondo alcuni, la clonazione di embrioni umani potrebbe rappresentare un approccio più diretto. Il dottor De Sousa, tuttavia, difende la necessità di mantenere aperte diverse possibilità nelle fasi iniziali della ricerca sulle cellule staminali, affermando: "Vogliamo queste linee cellulari essenzialmente a scopi di ricerca".
Le implicazioni legali sono diventate ancora più evidenti con le decisioni della Corte di giustizia dell'Unione europea. In un caso che rimanda a una sentenza del 2011, la Corte ha stabilito che un ovulo umano non fecondato, attivato per partenogenesi e che non possiede la capacità intrinseca di svilupparsi in un essere umano, può essere oggetto di brevetto a fini industriali o commerciali. Il criterio decisivo introdotto dalla Corte è la "capacità intrinseca di svilupparsi in un essere umano". Pertanto, il semplice fatto che un ovulo non fecondato inizi un processo di divisione cellulare non è sufficiente a qualificarlo come "embrione umano" ai fini della brevettabilità.
Questa sentenza ha modificato la precedente interpretazione, secondo cui anche gli ovuli non fecondati stimolati a svilupparsi tramite partenogenesi rientravano nella definizione di "embrione umano" e, di conseguenza, non potevano essere brevettati. La Corte ha chiarito che, se un ovulo non fecondato viene manipolato geneticamente in modo da poter svilupparsi in un essere umano, allora va considerato un embrione umano e, come tale, escluso dalla brevettabilità.
L'Avvocato Generale della Corte di Giustizia dell'UE, Pedro Cruz Villalón, ha espresso pareri secondo cui i partenoti, in quanto tali, non hanno la capacità di svilupparsi in un essere umano e dovrebbero quindi essere esclusi dalla definizione di embrione umano. Tuttavia, ha anche messo in guardia sulla possibilità che, in futuro, i partenoti umani possano essere alterati geneticamente per completare il loro sviluppo.
Le decisioni della Corte europea hanno sollevato preoccupazioni riguardo al potenziale aumento del commercio illegale di ovociti e all'espansione dell'area di brevettabilità e commercio di materiale biologico umano. L'opinione di Eugenia Roccella, deputata italiana, evidenzia il timore di una crescente confusione su cosa definisca l'umano e il rischio di un "assedio alle parti del corpo umano attraverso i processi tecnologici per arrivare alla commercializzazione".
Gravidanze Anembrionarie: Quando lo Sviluppo si Interrompe
È importante distinguere la ricerca sulla partenogenesi artificiale da condizioni mediche come la gravidanza anembrionaria, comunemente nota come "uovo chiaro". In questo scenario, che si verifica nelle prime fasi della gravidanza, l'ovulo fecondato si impianta nell'utero, e il sacco gestazionale si sviluppa, ma al suo interno non è presente alcun embrione o l'embrione smette di svilupparsi molto presto.
Le cause principali di una gravidanza anembrionaria sono anomalie cromosomiche nell'ovulo fecondato, che impediscono un corretto sviluppo fin dall'inizio. I sintomi iniziali possono essere simili a quelli di una gravidanza normale, come lieve sanguinamento o una diminuzione dei sintomi tipici come nausea o stanchezza, ma tendono a scomparire man mano che i livelli dell'ormone hCG diminuiscono.
La diagnosi di gravidanza anembrionaria viene solitamente confermata tramite ecografia tra la settima e la nona settimana di gestazione, quando si osserva un sacco gestazionale vuoto. Una volta diagnosticata, è necessario procedere all'espulsione del contenuto uterino. Questo può avvenire tramite l'uso di farmaci (come il misoprostolo), procedure chirurgiche come il raschiamento o l'aspirazione manuale, o, in alcuni casi, attendendo che il corpo espella naturalmente il sacco.
Le anomalie cromosomiche che portano a gravidanze anembrionarie possono essere identificate attraverso la Diagnosi Genetica Preimpianto (DGP), una tecnica utilizzata nella fecondazione in vitro (FIV) per analizzare geneticamente gli embrioni prima dell'impianto. La DGP mira a selezionare embrioni con una dotazione cromosomica normale, riducendo il rischio di gravidanze anembrionarie e altri problemi genetici.
La Fecondazione In Vitro: Tecniche e Sfide
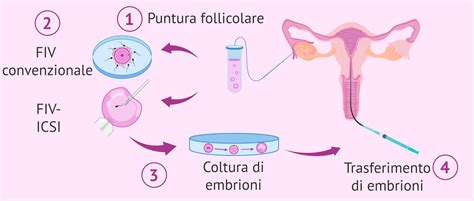
La fecondazione in vitro (FIV) rappresenta un pilastro della medicina riproduttiva assistita. Nel processo di FIV "convenzionale", ovuli e spermatozoi vengono messi in contatto in laboratorio, con l'obiettivo che uno spermatozoo penetri naturalmente nell'ovulo per fecondarlo. Tuttavia, questo processo non sempre ha successo, spesso a causa di problemi legati alla qualità degli spermatozoi o degli ovuli.
Quando la FIV convenzionale non è praticabile, si ricorre a tecniche più avanzate come la ICSI (Iniezione Intracitoplasmatica dello Spermatozoo). Nella ICSI, uno spermatozoo selezionato viene iniettato direttamente all'interno di un ovulo maturo, utilizzando una micropipetta. Questo metodo è particolarmente indicato in casi di infertilità maschile severa o quando la FIV convenzionale ha fallito in precedenza.
Nonostante l'efficacia di queste tecniche, è importante notare che la fecondazione non è garantita in tutti i casi. Possono verificarsi fecondazioni anomale, come la presenza di un solo pronucleo (invece dei due attesi, uno da parte materna e uno paterna), tre o più pronuclei, o, al contrario, ovuli non fecondati privi di qualsiasi pronucleo. In alcuni casi, vengono impiegati processi di attivazione per incrementare i tassi di fecondazione.
Conclusioni Preliminari: Un Territorio in Continua Evoluzione
La ricerca sull'ovulo umano non fecondato e la sua potenziale induzione alla divisione cellulare attraverso la partenogenesi artificiale rappresentano un campo di indagine scientifica all'avanguardia, ricco di promesse terapeutiche ma anche carico di interrogativi etici e legali. Le scoperte del gruppo di Paul de Sousa e le sentenze della Corte di giustizia dell'Unione europea delineano un paesaggio in rapida evoluzione, dove le capacità scientifiche si scontrano con la necessità di definire i confini della vita umana e di proteggere la dignità individuale.
Mentre la scienza continua a esplorare le frontiere della biologia riproduttiva, il dibattito pubblico e politico assume un ruolo cruciale nel guidare questa ricerca verso applicazioni responsabili e benefiche per la società, mantenendo sempre un occhio vigile sui rischi di commercializzazione e manipolazione che potrebbero minare i principi etici fondamentali. La discussione su cosa costituisca un "embrione umano" e su quali siano le implicazioni della sua creazione artificiale è destinata a proseguire, plasmando il futuro della ricerca biomedica e la nostra comprensione della vita stessa.

