Il neon, identificato nella tavola periodica degli elementi con il simbolo chimico Ne e numero atomico 10, è un elemento affascinante appartenente al gruppo dei gas nobili. La sua natura quasi inerte, unita alla sua distintiva luminescenza, lo ha reso protagonista di numerose applicazioni scientifiche e tecnologiche, dall'illuminazione pubblica alla ricerca medica avanzata. Questo articolo esplora in dettaglio il simbolo chimico del neon, le sue proprietà intrinseche, la sua scoperta e il suo impiego in vari settori, offrendo una panoramica completa di questo elemento essenziale.
Origini del Nome e Scoperta
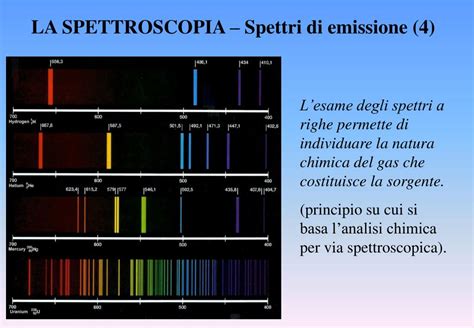
Il nome "neon" deriva dal greco antico "neos" (νέος), che significa "nuovo". Questa etimologia riflette la sua scoperta relativamente recente rispetto ad altri elementi più comuni. L'esistenza del neon fu prevista nel 1896 da Sir William Ramsay, in seguito alla sua scoperta dell'elio e dell'argon. Ramsay, insieme al suo collega Morris W. Travers, riuscì infine a identificare e isolare il neon nel 1898, attraverso la distillazione frazionata dell'aria liquida. La sua identificazione spettroscopica confermò la sua natura di nuovo elemento.
Posizione nella Tavola Periodica e Natura Chimica
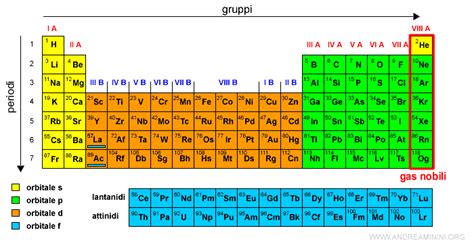
Il neon si colloca all'ultimo posto del secondo periodo della tavola periodica, precedendo il fluoro e seguendo l'elio. Appartiene al gruppo 18, noto come i gas nobili, caratterizzato da una configurazione elettronica esterna completa (2s²2p⁶), che conferisce loro una notevole stabilità e una scarsa reattività chimica. Questo rende il neon un gas quasi inerte, incapace di formare composti chimici stabili in condizioni normali. La sua elevata stabilità è ulteriormente sottolineata dal suo alto potenziale di ionizzazione, secondo solo a quello dell'elio, che ammonta a 21,5645 eV. Anche la sua affinità protonica è significativa (198,8 kJ/mol), indicando la sua capacità di accettare un protone, sebbene richieda condizioni relativamente blande per essere protonato.
Isotopi del Neon
Il neon presenta almeno 19 isotopi conosciuti, con numeri di massa che variano da A = 16 ad A = 34. Tra questi, tre isotopi sono stabili: ²⁰Ne, ²¹Ne e ²²Ne. L'analisi della composizione isotopica di questi tre isotopi stabili è fondamentale per distinguere il neon di origine terrestre (primordiale) da quello di altre fonti, come quelle extraterrestri o cosmogeniche. Un team di ricercatori dell'Università di Osaka ha recentemente fornito prove sperimentali dell'esistenza di stati eccitati nel nucleo di ²⁰Ne, osservando specifici stati energetici attraverso l'analisi dei prodotti di decadimento derivanti dall'irradiazione di gas neon con particelle alfa.
Proprietà Fisiche
Il neon è un gas monoatomico, incolore e inodore a temperatura e pressione ambiente. La sua densità è di circa 0,899 kg/m³ a 0°C e 1 atm. Possiede un bassissimo punto di ebollizione, pari a -246 °C, e il suo stato liquido ha una densità di 1,21 g/cm³. Il neon è insolubile in acqua.
La proprietà più distintiva del neon, e quella che ne ha determinato l'ampio utilizzo, è la sua capacità di emettere una caratteristica luce rosso-arancione quando attraversato da una scarica elettrica. Questa luminescenza è la base del suo impiego nelle lampade "al neon", che sono generalmente piccole e operano tra 100 e 250 volt. Sebbene il termine "neon" sia comunemente associato a queste luci, è importante notare che diversi gas vengono utilizzati per ottenere una vasta gamma di colori, con il neon puro che produce la tonalità rosso-arancione.
Applicazioni del Neon
Le applicazioni del neon sono molteplici e spaziano in diversi settori:
Illuminazione: Le lampade al neon sono state ampiamente utilizzate come indicatori di accensione e in apparecchiature di test dei circuiti. Sebbene siano state in gran parte sostituite dai diodi a emissione di luce (LED), le insegne al neon continuano a essere un elemento iconico in molte città per la loro distintiva luminosità.
Storia dell'illuminazione al neon | Podcast Ancestral Findings
Refrigerazione: Il neon liquido possiede una capacità di refrigerazione notevolmente superiore a quella dell'elio liquido e dell'idrogeno liquido, a parità di volume. Questo lo rende un refrigerante efficiente e, in molte applicazioni, più economico rispetto all'elio.
Medicina e Ricerca Scientifica:
- Radioterapia: La radioterapia con ioni di neon offre vantaggi sia biologici che fisici rispetto ai raggi X. Biologicamente, il fascio di neon riduce il rapporto di potenziamento dell'ossigeno e aumenta l'efficacia biologica relativa, portando a una minore variazione nella radiosensibilità cellulare e a una riduzione della riparazione dei danni da radiazioni. Sebbene il trattamento di alcuni tumori maligni con questa tecnica abbia mostrato efficacia limitata, la ricerca continua.
- Traccianti Radioattivi: L'isotopo radioattivo ²¹Ne viene impiegato come tracciante radioattivo in diverse ricerche.
- Laser: Il neon trova applicazione nei laser, in particolare nei laser a elio-neon (He-Ne), che sono stati storicamente importanti per le loro applicazioni in metrologia, spettroscopia e lettori di codici a barre.
Industria: Il neon viene utilizzato in valvole termoioniche, indicatori ad alta tensione, parafulmini, tubi per misuratori d'onda e nei tubi catodici.
Atmosfere Artificiali: In combinazione con l'ossigeno, il neon può fungere da gas diluente nelle atmosfere artificiali delle cabine spaziali, contribuendo a mantenere un ambiente respirabile per gli astronauti.
Curiosità sul Neon
Il termine "neon" non si limita all'elemento chimico. Nel linguaggio comune, "neon" si riferisce spesso alle lampade che emettono luce rossa-arancione, indipendentemente dal gas in esse contenuto. Inoltre, il termine "neon" o "neo" deriva dal greco "neos", che significa "nuovo", sottolineando la sua scoperta relativamente tardiva.
Conclusioni Parziali
Il neon, con il suo simbolo chimico Ne, rappresenta un elemento di grande interesse scientifico e tecnologico. Dalla sua scoperta alla sua vasta gamma di applicazioni, questo gas nobile continua a illuminare il nostro mondo, letteralmente e metaforicamente, attraverso le sue proprietà uniche e la sua crescente importanza in settori all'avanguardia. La sua quasi inerzia chimica, unita alla sua distintiva luminescenza, lo rende un componente prezioso in numerose tecnologie, dalla segnaletica luminosa alla medicina nucleare.

