La danza della vita inizia con un singolo evento: la fusione di due cellule altamente specializzate, un ovocita e uno spermatozoo, che dà origine allo zigote. Questa singola cellula, dotata di una straordinaria totipotenza, porta in sé il potenziale per svilupparsi in un organismo completo e perfettamente funzionante. Man mano che lo sviluppo procede, una serie di divisioni cellulari programmate porta alla progressiva acquisizione di identità cellulari e molecolari distinte, e la totipotenza si restringe fino a raggiungere la pluripotenza. Questo percorso verso la pluripotenza è guidato da una complessa modulazione del trascrittoma e dal rimodellamento del panorama epigenetico della cromatina, a cui contribuiscono anche modulatori esterni. Sia gli embrioni umani che quelli murini sono una fonte di diversi tipi di cellule staminali pluripotenti, le cui caratteristiche possono essere catturate e mantenute in vitro.
L'Essenza della Potenza Cellulare: Dalla Totipotenza alla Pluripotenza
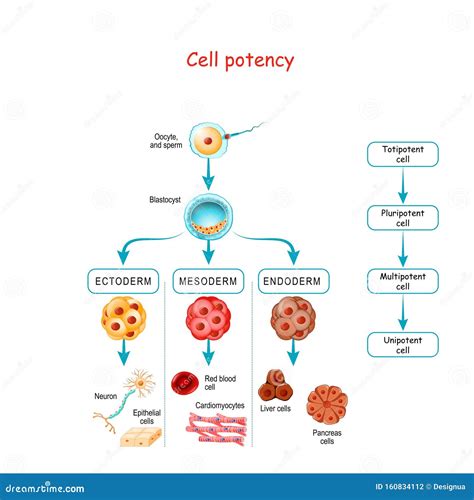
La capacità di una cellula di differenziarsi e dare origine a diversi tipi di cellule specializzate definisce la sua "potenza". A seconda del potenziale di differenziazione, la potenza spazia dalla totipotenza, pluripotenza, multipotenza, oligo- o unipotenza. La totipotenza, la forma più elevata di potenza, è la capacità di una cellula di generare non solo tutte le cellule del corpo, ma anche tutti i tessuti extraembrionali, come il trofoblasto che formerà la placenta e altre strutture essenziali per lo sviluppo embrionale.
Nei mammiferi, la vera totipotenza è strettamente limitata allo zigote e alle primissime divisioni cellulari, tipicamente fino allo stadio di 2 cellule e, in alcuni casi, fino allo stadio di 4 cellule. Dopo questi primi stadi, le cellule perdono la totipotenza e transitano verso la pluripotenza. La pluripotenza è la capacità di una cellula di dare origine a tutti i tipi di cellule che compongono i tre foglietti germinativi (ectoderma, mesoderma ed endoderma), ma non ai tessuti extraembrionali. Le cellule staminali pluripotenti, come quelle presenti nella massa cellulare interna (ICM) della blastocisti, possiedono questa capacità. Le cellule multipotenti, come le cellule staminali ematopoietiche, possono invece auto-rinnovarsi e differenziarsi in tipi cellulari specializzati all'interno di organi o tessuti specifici.
La transizione dalla totipotenza alla pluripotenza è un processo finemente regolato da cambiamenti nell'espressione genica e da modificazioni epigenetiche, tra cui la metilazione del DNA e la modificazione degli istoni. Fattori di trascrizione chiave, come Oct4, Sox2 e Nanog, diventano sovraregolati man mano che le cellule perdono totipotenza e acquisiscono pluripotenza.
Lo Stadio di Morula: Un Crogiolo di Destini Cellulari
Lo stadio di morula, che si verifica tipicamente intorno all'ottava cellula negli esseri umani (circa 3 giorni post-fecondazione) e a 2.5 giorni post-coito nei topi, rappresenta una fase cruciale nello sviluppo embrionale precoce. È uno stadio caratterizzato da un ammasso compatto di cellule che hanno subito una serie di divisioni mitotiche dallo zigote. Durante questo periodo, i blastomeri iniziano a perdere la loro totipotenza e a prepararsi per la successiva specificazione del lignaggio.
Nel topo, a partire dallo stadio di 8 cellule, gli embrioni subiscono la compattazione. Questo processo è indotto dall'assemblaggio dei complessi di polarità cellulare sulla membrana apicale esterna dei blastomeri e dalla localizzazione di specifiche proteine sulla membrana basolaterale di ciascun blastomero, generando un asse apicale-basale. Contemporaneamente alla polarizzazione, l'espressione e la localizzazione di E-caderina e di diverse proteine legate al citoscheletro e alle giunzioni cellulari permettono la compattazione dell'embrione. A questo punto, un interruttore da divisioni cellulari tutte simmetriche a divisioni combinate simmetriche e asimmetriche genera un embrione morula con cellule polari esterne e cellule apolari interne.
Dallo stadio di morula, la specificazione del lignaggio e la differenziazione sono accompagnate da una diminuzione della potenza cellulare globale. La prima specificazione del lignaggio è determinata da diversi percorsi regolatori, tra cui il pathway di segnalazione Hippo, che svolge un ruolo importante nell'innescare la specificazione dell'ICM e del trofoblasto (TE). Il pathway Hippo è selettivamente inattivo nelle cellule esterne e attivo nelle cellule interne dell'embrione. Nelle cellule esterne, Yap1 e la sua proteina correlata Wwtr1 (d'ora in poi chiamata Yap) traslocano e si accumulano nel nucleo, dove attivano il programma trascrizionale specifico del TE. Yap1 promuove l'espressione di Cdx2 e Gata-3, che, insieme a Notch, Eomes e Elf5, contribuiscono alla sua differenziazione e inducono il destino del TE, mentre reprimono l'espressione di Sox2. Nelle cellule interne, Yap1 viene fosforilato e trattenuto nel citoplasma, dove viene degradato; così, il pathway Hippo viene attivato, consentendo la trascrizione di geni specifici dell'ICM (ad esempio, Oct-4, Nanog, Sox2 ed Esrrb).
Negli embrioni umani, la polarizzazione, che inizia allo stadio di 8 cellule, e la compattazione portano allo stadio di morula (4 giorni post-fecondazione, dpf). I meccanismi molecolari che guidano questi processi nell'uomo sono ancora poco chiari, ma poiché sono altamente conservati in tutte le specie di mammiferi (ad eccezione della tempistica), si ipotizza che la compattazione dei blastomeri umani sia guidata dal citoscheletro di actomiosina e dalla E-caderina, come in altre specie. Al momento in cui gli embrioni raggiungono la compattazione, sono state osservate espressioni di microvilli apicali e di E-caderina basolaterale.
Attivazione del Genoma Embrionale e Prime Specificazioni del Lignaggio
Immediatamente dopo la fecondazione, lo sviluppo ulteriore dello zigote totipotente è controllato da fattori di effetto materno (RNA e proteine) accumulati durante la maturazione dell'ovocita, che governano la transizione materno-embrionale e la successiva attivazione del genoma embrionale (EGA). L'EGA è un passaggio obbligatorio per la sintesi di nuove trascrizioni necessarie all'acquisizione di un controllo embrionale dello sviluppo.
Nel topo, una piccola ondata di EGA inizia nello zigote nella fase S/G2, seguita da un'ondata maggiore allo stadio di 2 cellule. Quando inizia la trascrizione genomica, i satelliti maggiori vengono attivati massicciamente, insieme agli elementi trasponibili (TE). Questi ultimi comprendono elementi nucleari interspaziati lunghi 1 (LINE-1), particelle intracisternali A (IAP) e retrovirus endogeni murini con primer tRNA per la leucina (MuERV-L). Le trascrizioni dei TE, con diverse cinetiche di espressione, costituiscono una porzione significativa del trascrittoma durante l'EGA murino. L'EGA coincide con la degradazione graduale e progressiva delle trascrizioni materne. Diversi complessi proteici leganti l'RNA regolano il silenziamento dell'mRNA materno per promuoverne la degradazione tramite clivaggio, de-adenilazione ed eliminazione del loro cap protettivo. La precoce espressione di microRNA zigotici è necessaria per la degradazione di centinaia di trascrizioni materne. Inoltre, specifici fattori di trascrizione, ad esempio il fattore generale di trascrizione TATA-binding protein, parte del complesso TFIID, promuovono la formazione del complesso di pre-iniziazione della RNA polimerasi II, dirigendo il macchinario trascrizionale durante l'EGA. La sinergia tra EGA e degradazione dell'RNA induce il rimodellamento genomico, mediato da acetilazione e metilazione degli istoni, dall'instaurazione di domini topologicamente associati e dal posizionamento dei nucleosomi, obbligatorio per l'acquisizione dell'identità cellulare nell'embrione. Dopo l'EGA, sorgono differenze molecolari tra i blastomeri.
Negli embrioni umani, si osservano due ondate di EGA: una ondata minore allo stadio di 2 cellule e un'ondata maggiore tra lo stadio di 4 e 8 cellule. L'EGA coincide con la degradazione graduale delle trascrizioni materne e, come riportato per il topo, i TE (SINE-VNTR-Alus; HERV) vengono pesantemente trascritti.
La Morula in Italia: Ricerca e Innovazione
La ricerca italiana ha dato contributi significativi alla comprensione dello sviluppo embrionale precoce. Un team di ricercatori dell'Università di Torino, in collaborazione con l'Università di Padova, ha ricreato in laboratorio un modello tridimensionale di embrione umano utilizzando cellule staminali. Nelle fasi più precoci della formazione embrionale, le cellule si dispongono in uno strato ordinato, creando una piccola cavità interna, una sorta di sfera cava, che diventerà la futura cavità amniotica.
Poiché i segnali che guidano questi processi nell'embrione umano sono ancora in gran parte sconosciuti, i ricercatori hanno utilizzato tecniche avanzate di genomica e editing genetico per identificarli. Il team ha scoperto che un segnale di comunicazione cellula-cellula chiamato TGF-beta coordina le fasi più precoci dell'organizzazione cellulare e la formazione della cavità amniotica, attraverso un gene regolatore chiave, ZNF398, che controlla molti altri geni coinvolti nella costruzione della struttura tridimensionale dell'embrione. Successivamente, un segnale simile, Activin A, innesca le migrazioni cellulari e i processi di differenziazione necessari per la formazione degli organi.
Embrione blastocisti: Cos’è, vantaggi, tipi e classificazione in base alla sua qualità
Questi modelli sperimentali, come quello sviluppato a Torino e Padova, sono altamente affidabili e facilmente riproducibili, poiché ogni componente è stato definito con precisione. Oltre a chiarire i segnali che guidano lo sviluppo embrionale, questi modelli rendono possibile comprendere quali nutrienti sono essenziali in queste fasi precoci o quali farmaci potrebbero interferire con essi.
Sfide Tecniche ed Etiche nella Manipolazione delle Cellule Staminali Totipotenti
L'isolamento e il mantenimento delle cellule staminali totipotenti in laboratorio presentano notevoli ostacoli. Queste cellule sono estremamente sensibili e richiedono condizioni precise per mantenere la vitalità in vitro. Le cellule staminali totipotenti esistono solo transitoriamente in vivo, principalmente nello zigote e negli stadi precoci di clivaggio (da 2 a 4 cellule), rendendo il loro isolamento intrinsecamente difficile. Inoltre, il mantenimento della loro condizione indifferenziata richiede l'avvio di fasi di sviluppo precoci, poiché le cellule totipotenti si differenziano spontaneamente immediatamente dopo la fecondazione. Sistemi di coltura in vitro in grado di sostenere in modo affidabile la totipotenza per periodi prolungati non sono ancora stati completamente stabiliti, a differenza delle cellule staminali pluripotenti, che possono essere coltivate a lungo termine. La ragione principale di ciò è il tasso di crescita apparentemente lento osservato in tutte le cellule staminali totipotenti riportate finora.
Le questioni etiche relative all'uso delle cellule staminali totipotenti si concentrano sugli embrioni umani. La maggior parte delle persone considera l'uso di embrioni umani nella ricerca una preoccupazione morale perché li distrugge, mentre altri credono che i possibili vantaggi medici lo giustifichino. Ciò suscita dibattiti sullo status morale dell'embrione, con alcuni che lo considerano dotato di pieni diritti umani fin dal concepimento, mentre altri lo considerano un ammasso di cellule fino a fasi successive di sviluppo. Esistono anche preoccupazioni riguardo al potenziale di clonazione umana o di uso improprio nella modificazione genetica.
Quadri etici come la "regola delle 14 giorni" limitano la ricerca sugli embrioni umani oltre i 14 giorni post-fecondazione, quando si forma la stria primitiva, segnando l'inizio dello sviluppo individuale. Queste considerazioni etiche continuano a suscitare dibattiti in circoli scientifici, religiosi e politici. Organizzazioni internazionali come la International Society for Stem Cell Research (ISSCR) forniscono linee guida per garantire una condotta etica nella ricerca sulle cellule staminali.
Le politiche sull'uso delle cellule staminali variano significativamente tra i paesi. Ad esempio, in Italia, le leggi sono restrittive riguardo alla ricerca sulle cellule staminali embrionali. Al contrario, paesi come il Regno Unito e il Canada consentono ricerche regolamentate sotto sistemi di licenza. La percezione pubblica della ricerca sulle cellule staminali, incluso l'uso di cellule staminali totipotenti, gioca un ruolo critico nel plasmare le politiche e le decisioni di finanziamento.
Prospettive Future nella Ricerca sulle Cellule Staminali Totipotenti
Il futuro della ricerca sulle cellule staminali totipotenti è ricco di prospettive promettenti. I progressi nell'editing genetico, come CRISPR-Cas9, offrono entusiasmanti prospettive per migliorare la capacità delle cellule staminali totipotenti di rigenerare tessuti o trattare disturbi genetici. Queste tecnologie consentono un controllo più preciso della differenziazione cellulare e possono aumentare la sicurezza e l'efficacia delle terapie basate su cellule staminali.
Progressi recenti nel sequenziamento a singola cellula e nella profilazione molecolare stanno fornendo intuizioni più profonde sulle reti di regolazione genica e sui paesaggi epigenetici che distinguono le cellule totipotenti dalle cellule pluripotenti e multipotenti. La capacità di generare cellule simili a quelle totipotenti da tessuti adulti potrebbe portare a scoperte significative nella medicina personalizzata, fornendo ai pazienti terapie personalizzate derivate dalle loro cellule. Le applicazioni emergenti includono modelli embrionali sintetici e organoidi multi-linaggio per la modellazione di malattie, la scoperta di farmaci e studi sullo sviluppo.
Nonostante questi progressi, rimangono sfide nel controllare con precisione la differenziazione delle cellule totipotenti, garantirne la sicurezza e affrontare le preoccupazioni etiche relative alla creazione e all'uso di costrutti simili a embrioni umani. Le cellule staminali totipotenti sono fondamentali per la comprensione dello sviluppo embrionale precoce, della differenziazione cellulare e delle origini della vita. Offrono inoltre potenziali applicazioni nelle tecnologie di clonazione, migliorando la nostra conoscenza degli aborti spontanei e dei difetti dello sviluppo, e facendo progredire la medicina rigenerativa scoprendo come le cellule diventano specializzate.
La ricerca sulle cellule staminali totipotenti, in particolare a stadi precoci come la morula, continua ad essere un campo dinamico e in rapida evoluzione, con il potenziale di rivoluzionare la nostra comprensione della biologia dello sviluppo e di aprire nuove frontiere terapeutiche.
tags: #staminali #embrionali #stadio #di #morula

