La prospettiva di creare ovuli umani completamente funzionali a partire da cellule della pelle non è più confinata nel regno della fantascienza. Ricerche pionieristiche stanno aprendo scenari rivoluzionari nel trattamento dell'infertilità, offrendo nuove speranze a individui e coppie che affrontano sfide riproduttive. Questo campo emergente, noto come gametogenesi in vitro (IVG), mira a produrre gameti - ovuli e spermatozoi - in laboratorio, utilizzando il DNA del paziente stesso. Le implicazioni scientifiche, etiche e sociali di questi progressi sono profonde e meritano un'analisi approfondita.
Le Sfide dell'Infertilità e le Tecniche Riproduttive Attuali
A livello globale, l'infertilità colpisce una percentuale significativa della popolazione adulta, con oltre 13 milioni di bambini nati grazie alle tecniche di riproduzione assistita negli ultimi anni. La fecondazione in vitro (FIV) rimane la procedura più diffusa, ma non sempre è efficace. Le ragioni del fallimento possono essere molteplici, tra cui la qualità degli ovuli, che tende a diminuire con l'avanzare dell'età, o problemi legati ai trattamenti oncologici e ad altre condizioni mediche.
Le opzioni attuali includono il trasferimento mitocondriale, che aiuta a prevenire la trasmissione di malattie mitocondriali ereditarie, e l'uso di ovuli o spermatozoi donati quando le riserve genetiche sono compromesse. Tuttavia, la gametogenesi in vitro rappresenta un passo avanti significativo, promettendo soluzioni più personalizzate e innovative, potenzialmente riducendo la dipendenza dalla donazione di gameti.
Dalla Pelle all'Ovulo: La Tecnica Rivoluzionaria
Al centro di questa nuova frontiera si trova il trasferimento nucleare di cellule somatiche (SCNT), una tecnica simile a quella impiegata per la clonazione della pecora Dolly. Il processo prevede l'estrazione del nucleo da una cellula somatica (come una cellula della pelle) e il suo inserimento in un ovulo donatore precedentemente privato del proprio materiale genetico. L'obiettivo è creare un ovulo funzionante che porti il materiale genetico del futuro genitore.
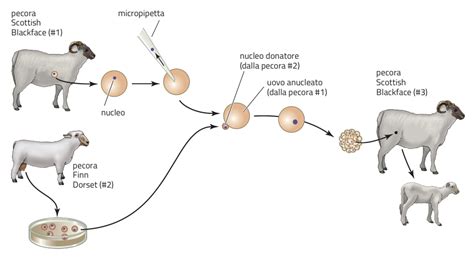
Una delle sfide più significative è che le cellule somatiche contengono 46 cromosomi, mentre ovuli e spermatozoi ne possiedono solo 23. Per superare questo ostacolo, i ricercatori hanno sviluppato un processo chiamato "mitomeiosi", un meccanismo di divisione cellulare artificiale che imita il processo naturale di riduzione cromosomica. Questo passaggio è cruciale per ottenere una cellula aploide pronta per la fecondazione, garantendo la formazione di embrioni sani con il corretto numero di cromosomi. La dimostrazione di questa tecnica negli esseri umani, dopo esperimenti riusciti nei topi, segna un traguardo fondamentale.
I Risultati della Ricerca: Successi e Limiti
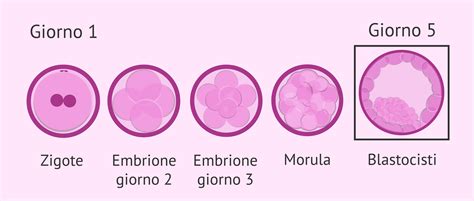
Negli esperimenti condotti, i ricercatori sono riusciti a generare 82 ovuli funzionali, che sono stati poi fecondati con sperma in laboratorio. Circa il 9% di questi ovuli ha raggiunto lo stadio di blastocisti, una fase cruciale nello sviluppo embrionale che precede il trasferimento nell'utero. Sebbene questo tasso di successo indichi che il processo non è ancora pienamente efficiente, rappresenta una "prova di concetto" significativa.
Tuttavia, nessuno degli embrioni ottenuti ha mostrato un corretto allineamento cromosomico. Questo problema è legato alla complessa natura della meiosi umana, il processo di divisione cellulare che dimezza il numero di cromosomi. La mitomeiosi, pur replicando alcuni aspetti di questo processo, non è ancora in grado di garantire la corretta segregazione dei cromosomi. Il professor Shoukhrat Mitalipov, a capo del team di ricerca, ha sottolineato che perfezionare la tecnica e garantirne la sicurezza richiederà ancora molti anni di lavoro.
Il Ruolo Cruciale della Microscopia a Luce Polarizzata
Nella gestione clinica degli ovociti, tecniche come la microscopia a luce polarizzata (PLM) giocano un ruolo fondamentale. La PLM consente di verificare in modo non invasivo se l'ovocita ha completato la maturazione nucleare e ha assemblato il fuso meiotico II (MII). L'identificazione di un fuso bipolare è associata a una maggiore competenza di sviluppo dell'embrione.
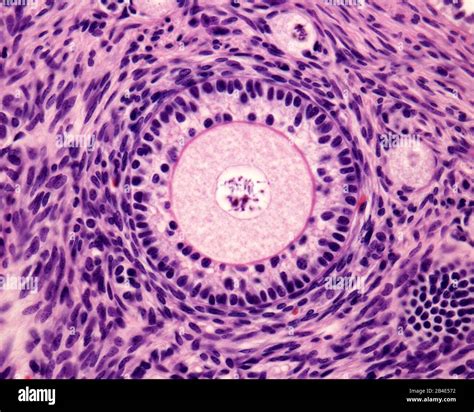
Questa tecnica è particolarmente utile per discriminare gli ovociti che potrebbero essere arrestati nella fase MII da quelli che stanno attraversando una transizione maturazionale importante, specialmente in casi di maturazione ritardata. La rimozione delle cellule follicolari e l'incubazione separata degli ovociti a diversi stadi di maturazione possono facilitare la distinzione tra ovociti maturati in vivo e quelli che completano la maturazione in vitro. Comprendere le dinamiche del fuso durante la maturazione meiotica è essenziale per interpretare correttamente i segnali PLM. Ad esempio, l'assenza transitoria del segnale del fuso durante l'intercinesi non indica necessariamente un disturbo cellulare, ma potrebbe segnalare la progressione da MI a MII. Il rinvio dell'iniezione spermatica in caso di ovociti a maturazione tardiva permette loro di assemblare un fuso MII, migliorando i risultati clinici. Studi hanno dimostrato che una percentuale significativa di ovociti inizialmente negativi al segnale del fuso sviluppa tale segnale entro poche ore.
Oltre la Maturità: Imaging del Fuso e Biopsia
L'imaging del fuso è raccomandato anche prima della biopsia del corpo polare (PB) per evitare la distruzione del fuso in ovociti in anafase/telofase. La classificazione degli ovociti basata sul modello PLM, che varia da un segnale prominente del fuso bipolare a nessun fuso rilevabile, fornisce informazioni preziose sulla loro competenza.
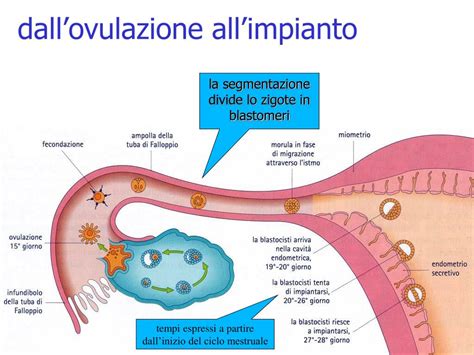
La correlazione tra l'organizzazione cromosomico-microtubulare e il pattern di birifrangenza rilevato dalla PLM è un'area di ricerca attiva. Sebbene la PLM possa rilevare la presenza di un fuso, non sempre garantisce l'allineamento corretto dei cromosomi. La ricerca sta esplorando come associare i segnali PLM con l'accuratezza dell'organizzazione cromosomica per una valutazione più completa dell'idoneità dell'ovocita.
Prospettive Future e Considerazioni Etico-Legali
La capacità di creare ovuli da cellule della pelle apre scenari rivoluzionari:
- Trattamento dell'infertilità: Potrebbe offrire una soluzione per donne con riserva ovarica ridotta, età materna avanzata, o che hanno subito trattamenti oncologici.
- Coppie dello stesso sesso: Permetterebbe a coppie omosessuali di avere figli geneticamente legati a entrambi i partner.
- Riduzione della dipendenza da donatori: Diminuirebbe la necessità di ovociti e spermatozoi donati.
Tuttavia, la strada verso l'applicazione clinica è ancora lunga e presenta numerose sfide:
- Sicurezza ed Efficacia: La mitomeiosi deve essere perfezionata per garantire un corretto numero e allineamento cromosomico, evitando aberrazioni genetiche. La sicurezza a lungo termine degli embrioni e dei potenziali discendenti deve essere rigorosamente valutata.
- Questioni Etiche e Legali: La creazione e manipolazione di embrioni solleva interrogativi complessi riguardo allo status morale dell'embrione, alla definizione di genitorialità e al potenziale uso per scopi non terapeutici, come la selezione di tratti desiderabili. Le normative variano significativamente tra i paesi, con alcune giurisdizioni che vietano la ricerca su embrioni umani e altre che la consentono, ma con restrizioni sull'applicazione clinica.
La Riproduzione Assistita: tecnologie d’avanguardia e riflessi psicologici, bioetici e sociali
La ricerca sulla gametogenesi in vitro, sebbene ancora nelle sue fasi iniziali, rappresenta un avanzamento scientifico di notevole importanza. La trasparenza con cui i ricercatori stanno condividendo i loro risultati, inclusi i limiti attuali, è fondamentale per un dibattito informato. Mentre la creazione di ovuli umani da cellule della pelle non è ancora una terapia pronta per l'uso clinico, essa simboleggia un passo cruciale nella nostra comprensione della biologia riproduttiva e nella potenziale risoluzione di complesse sfide legate all'infertilità. Il percorso richiederà ancora anni di ricerca rigorosa, ma la promessa di un futuro in cui la riproduzione assistita possa essere più accessibile e personalizzata è una prospettiva incoraggiante.
Il Contesto Normativo e le Prospettive Globali
Le implicazioni normative della gametogenesi in vitro sono altrettanto complesse quanto quelle scientifiche. In Italia, ad esempio, la Legge 40/2004 impone restrizioni severe sull'uso degli embrioni e sulla procreazione medicalmente assistita. A livello europeo e statunitense, l'impianto di embrioni derivati da esperimenti simili è generalmente vietato. La questione di chi debba essere considerato il "genitore biologico" quando i gameti sono creati artificialmente è un altro aspetto che richiederà un'attenta considerazione legale ed etica.
La ricerca di Katsuhiko Hayashi dell'Università di Osaka sui topi, che ha portato alla nascita di cuccioli da ovociti creati da cellule maschili, dimostra ulteriori progressi nel campo, aprendo la possibilità teorica di generare gameti da individui dello stesso sesso. Tuttavia, anche in questo caso, le implicazioni per la specie umana sono ancora lontane e controverse.
Nonostante le sfide, diverse startup negli Stati Uniti stanno attivamente lavorando allo sviluppo di ovuli e spermatozoi in laboratorio, indicando un crescente interesse commerciale e scientifico in questo campo. L'incremento della domanda di ovociti donati, dovuto alla crescente popolarità della FIV, sottolinea ulteriormente la potenziale necessità di alternative come la gametogenesi in vitro.
In conclusione, la creazione di ovuli umani da cellule della pelle rappresenta un affascinante avanzamento nella ricerca di base. Non è ancora una terapia rivoluzionaria pronta all'uso, ma una pietra miliare che promette di migliorare la nostra comprensione dei meccanismi biologici e, potenzialmente, di aprire nuove strade per il trattamento dell'infertilità in futuro. La scienza procede per passi incrementali, e ogni progresso tecnico, anche se inizialmente limitato, contribuisce a costruire le fondamenta per future innovazioni.

